Zycubo injection approved for the treatment of Menkes disease
संदर्भ:
हाल ही में अमेरिकी खाद्य एवं औषधि प्रशासन (FDA) ने Zycubo (कॉपर हिस्टिडिनेट) इंजेक्शन को मेंकेस रोग (Menkes Disease) से पीड़ित बच्चों के उपचार के लिए अपनी ऐतिहासिक मंजूरी दी है। यह दवा, मेंकेस रोग के लिए दुनिया की पहली और एकमात्र अनुमोदित चिकित्सा बन गई है।
मेंकेस रोग (Menkes Disease) के बारे में:
मेंकेस रोग एक दुर्लभ, घातक और अनुवांशिक विकार है जो शरीर में तांबे (कॉपर) के चयापचय (Metabolism) को बाधित करता है।
- कारण (Causative Gene): यह रोग ATP7A जीन में उत्परिवर्तन (Mutation) के कारण होता है। यह जीन शरीर के विभिन्न हिस्सों में तांबे के परिवहन और वितरण के लिए जिम्मेदार होता है।
- आनुवंशिकी (Genetics): यह एक X-लिंक्ड रिसेसिव (X-linked recessive) विकार है, जिसका अर्थ है कि यह मुख्य रूप से पुरुष शिशुओं को प्रभावित करता है।
- प्रभाव: आहार के माध्यम से प्राप्त तांबा आंतों में फंस जाता है और मस्तिष्क व अन्य महत्वपूर्ण अंगों तक नहीं पहुँच पाता। तांबे की कमी से मस्तिष्क का विकास रुक जाता है, हड्डियां कमजोर हो जाती हैं और रक्त वाहिकाएं असामान्य हो जाती हैं।
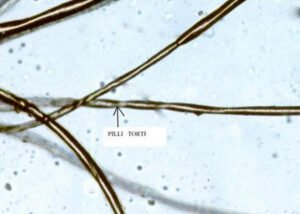
- लक्षण: इसे ‘किंकी हेयर डिजीज’ (Kinky Hair Disease) भी कहा जाता है क्योंकि प्रभावित बच्चों के बाल सफेद, विरल और मुड़े हुए होते हैं। अन्य लक्षणों में दौरे पड़ना (Seizures), मांसपेशियों में कमजोरी (Hypotonia) और विकास में देरी शामिल है।
Zycubo (कॉपर हिस्टिडिनेट):
Zycubo एक सबक्यूटोनियस (Subcutaneous – त्वचा के नीचे) इंजेक्शन है जो सीधे शरीर में तांबे की आपूर्ति करता है।
- मैकेनिज्म: यह दवा आंतों के उस दोष को बायपास कर देती है जो तांबे के अवशोषण को रोकता है, जिससे शरीर को सीधे आवश्यक तांबा प्राप्त होता है।
- महत्व: उपचार न मिलने पर बच्चे आमतौर पर 2 से 3 साल की उम्र तक ही जीवित रह पाते हैं। Zycubo ने नैदानिक परीक्षणों (Clinical Trials) में मृत्यु दर के जोखिम को 80% तक कम करने की क्षमता दिखाई है।
महत्वपूर्ण नैदानिक परिणाम:
FDA द्वारा दी गई यह मंजूरी दो ओपन-लेबल, सिंगल-आर्म परीक्षणों के डेटा पर आधारित थी:
- जीवित रहने की दर: जिन शिशुओं में जन्म के 4 सप्ताह के भीतर उपचार शुरू किया गया, उनकी उत्तरजीविता दर में भारी वृद्धि देखी गई।
- तुलनात्मक डेटा: अनुपचारित बच्चों की तुलना में, Zycubo लेने वाले बच्चों में औसत उत्तरजीविता (Median Survival) 17.6 महीने से बढ़कर 17.7 महीने से अधिक हो गई।
- दीर्घकालिक लाभ: उपचारित मरीजों में से लगभग आधे 6 साल से अधिक जीवित रहे, जबकि बिना उपचार वाले नियंत्रण समूह में कोई भी बच्चा 6 साल तक नहीं पहुंच सका।
FDA का विशेष पदनाम:
इस दवा की गंभीरता और दुर्लभता को देखते हुए, FDA ने इसे निम्नलिखित विशेष दर्जे प्रदान किए थे:
- ब्रेकथ्रू थेरेपी (Breakthrough Therapy): गंभीर स्थितियों के लिए त्वरित विकास हेतु।
- फास्ट ट्रैक (Fast Track): महत्वपूर्ण चिकित्सा जरूरतों को तेजी से पूरा करने के लिए।
- ऑर्फन ड्रग (Orphan Drug): दुर्लभ बीमारियों की दवाओं के लिए विशेष प्रोत्साहन।
- दुर्लभ बाल रोग पदनाम (Rare Pediatric Disease Designation): बच्चों में होने वाली दुर्लभ बीमारियों पर ध्यान केंद्रित करने के लिए।